ابتکار پژوهشگران چینی برای ترمیم آسیب نخاعی
ارتباط فردا: ماده زیستی جدیدی که توسط پژوهشگران «دانشگاه سیچوآن»(Sichuan University) ابداع شده است، میتواند التهاب و آسیب ناشی از حذف مولکولهای فعال اکسیژن را که در نتیجه آسیب نخاعی توسط بدن آزاد میشوند، کاهش دهد.
به نقل از ادونسد ساینس نیوز، «چونگ چنگ»(Chong Cheng)، استاد دانشگاه سیچوآن و سرپرست این پژوهش، گفت: آسیب نخاعی نشاندهنده یک مشکل مهم در سلامت جهانی است که بیش از ۲۰ میلیون نفر را در سراسر جهان تحت تأثیر قرار میدهد. درمان آسیب نخاعی به دلیل ظرفیت محدود بازسازی سلولهای عصبی چالشبرانگیز است که بیشتر توسط یک ریزمحیط نامطلوب با سطوح بالای گونههای اکسیژن فعال و التهاب محدود میشود.
اگرچه این پژوهش هنوز در مراحل اولیه است، اما نتایج آزمایش روی موشها بهبود قابل توجهی را در ترمیم و حرکت بافت پس از درمان با کمک این ماده نشان میدهند. اگر این نتایج در آزمایش انسانی تایید شوند، میتوانند یک روش جدید امیدوارکننده برای این نوع آسیب باشند.
آسیب نخاعی تروماتیک معمولا پس از تصادف با وسیله نقلیه یا سقوط رخ میدهد و دومین علت شایع فلج اندام پس از سکته مغزی است. به دلیل پیچیدگی بافت عصبی در ستون فقرات، درمان آسیب نخاعی دشوار است. چنگ گفت: مشکل درمان آسیبهای نخاعی به دلیل نقش نخاع به عنوان یک بزرگراه اطلاعاتی پیچیده است که رشتههای عصبی مهم و بیشماری را در یک فضای محدود حمل میکند. هنگامی که آسیب رخ میدهد، انتقال اطلاعات بلافاصله مختل میشود و ترمیم را بسیار چالشبرانگیز میکند. به دلیل محدودیت ظرفیت بازسازی سلولهای عصبی، این آسیب اغلب غیر قابل برگشت است.
مراحل متعددی برای این نوع آسیب وجود دارد، زیرا پس از ایجاد آسیب تروماتیک اولیه در یک ناحیه، آسیب ثانویه ایجاد میشود. تغییرات سلولی و مولکولی متعددی در بافت رخ میدهند که از دقایقی پس از آسیب آغاز میشوند و گاهی تا ماهها پس از آن ادامه مییابند و به آسیب پیشرونده و مرگ سلولی میانجامند.
پژوهشگران دههها تلاش کردهاند و نتوانستهاند درمانهایی را برای آسیب نخاعی ابداع کنند. چنگ توضیح داد: هدف درمان با جراحی، بازیابی و حفظ ثبات ستون فقرات از طریق تثبیت داخلی است، اما آسیبهای موجود یا پیشرونده را بررسی نمیکند.
درمان آسیب ثانویه دشوار است، اما در حال حاضر هیچ درمان مؤثر و تاییدشدهای برای مبارزه با این مشکل وجود ندارد. این مشکل تا حدی به دلیل پیچیدگی بافت و آسیب است. همچنین، آزمایشهای بالینی برای این نوع آسیب دشوار و پرهزینه هستند، زیرا به دلیل سرعت پایین بازسازی عصبی، به دورههای زمانی طولانی برای ارزیابی اثربخشی درمانها نیاز است.
چنگ گفت: «متیلپردنیزولون»(Methylprednisolone) تنها دارویی است که در حال حاضر در دستورالعملهای بالینی برای درمان آسیب نخاعی ثانویه توصیه میشود. با وجود این، استفاده از آن به دلیل لزوم تجویز زودهنگام با دوز بالا و درمان مداوم که میتواند به بروز عوارض جانبی قابل توجهی منجر شود، بحثبرانگیز است.
تجمع گونههای فعال اکسیژن در محل آسیب به بروز اثرات منفی از جمله آسیب اکسیداتیو به DNA، اکسیداسیون پروتئینها و پراکسیداسیون لیپیدی منجر میشود که همگی سلولهای عصبی آسیبدیده را به سمت مرگ سلولی سوق میدهند. تجمع گونههای فعال اکسیژن در ترکیب با التهاب – در صورت عدم کنترل – آسیب قابل توجهی را به بافت وارد میکند.
چنگ و همکارانش در این پژوهش، ماده خاصی را متشکل از فلز کمیاب روتنیوم و هیدروکسید مس که در کلاژن محصور شده است، ساختند. این ماده برای کاهش التهاب و مرگ سلولهای عصبی پس از آسیب نخاعی با حذف گونههای فعال اکسیژن اضافی از محل آسیب طراحی شده است. این ماده به عنوان یک پاککننده مولکولهای اکسیژن فعال اضافی در بافت عمل میکند و به طور مؤثر به پاکسازی آنها میپردازد.
«تینگ وانگ»(Ting Wang) از پژوهشگران این پروژه، گفت: کاوشگر ما به سرعت گونههای اکسیژن فعال مضر را از بین میبرد، مرگ نورونها را کاهش میدهد، ماکروفاژها را به اتخاذ یک فنوتیپ ضد التهابی وادار میکند و به محافظت از سلولهای مهم مانند سلولهای بنیادی عصبی و سلولهای بنیادی الیگودندروسیت میپردازد.
سایر گروههای پژوهشی نیز به دنبال استفاده از مولکولهای آنتی اکسیدان برای درمان آسیب نخاعی ثانویه هستند، اما چنگ معتقد است این ماده جدید نسبت به مولکولهای آنتی اکسیدان طبیعی مانند سوپراکسید دیسموتاز مزایایی دارد. همچنین، این ماده پایدارتر و برای دارورسانی آسانتر است و کمتر احتمال دارد که واکنشهای ایمنی نامطلوب را در بیماران ایجاد کند.
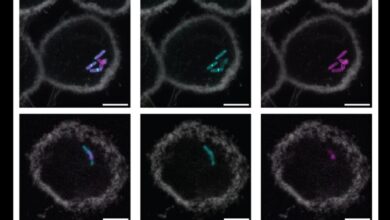
پژوهشگران این ماده را همراه با کلاژن و بدون کلاژن آزمایش کردند. پژوهشگران در بررسیهای آزمایشگاهی روی موشها نشان دادند که ماده جدید آنها میتواند مرگ سلولی ناشی از گونههای اکسیژن فعال اضافی را در سلولهای عصبی کاهش دهد و التهاب را در ناحیه آسیب کمتر کند.
موشهای تحت درمان با این ماده زیستی، ساختار نخاع و بازسازی سلولهای عصبی را بهتر از موشهای درماننشده بازیابی کردند. وانگ گفت: قابل ذکر است که با گذشت ۲۸ روز پس از آسیب، موشها در مقایسه با موشهای درماننشده بهبود قابل توجهی را در تحرک نشان دادند.
اگرچه نتایج این پژوهش امیدوارکننده هستند، اما این درمان هنوز راه زیادی را تا رسیدن به بیماران دارد. چنگ گفت: چالشهای فنی و نظارتی متعددی وجود دارند که در انتقال درمان از آزمایشگاه به آزمایشهای بالینی باید مورد توجه قرار بگیرند. ما متعهد هستیم که شرایط را برای بهینهسازی بیشتر راهبردهای درمانی به طور کامل بررسی کنیم.
این پژوهش در مجله «Advanced Materials» به چاپ رسید.
انتهای پیام